过去30年,技术飞速发展
30年来,消化内镜的发展对消化系统疾病的诊断和治疗起到了革命性的推动作用。消化内镜及其手术器械的更新促进了消化内镜技术的不断发展完善,诊断内镜“多样化”、治疗适应证“扩大化”是当前消化内镜的发展趋势。
1 电子内镜为新技术的发展奠定基础
消化内镜技术肇始于1868年,当时德国人库斯穆尔(Kussmaul)受江湖艺人吞剑表演的启示,研制出金属管状式胃镜。历经硬式内镜、半可屈式内镜、纤维内镜(软式镜)三个发展阶段后,消化内镜技术在30年前迎来了又一次革命性的飞跃。
1983年,美国一家公司应用电荷耦合器件(CCD)代替内镜光导纤维导像术,宣告了电子内镜的诞生。电子内镜的成像原理与传统内镜截然不同,其通过安装在内镜顶端微型摄像机的CCD,使光信号转变为电信号,经视频系统处理后转换为监视器上的图像。因此,电子内镜显像失真性小、清晰度高,为诊断和治疗创造良好条件,也为此后各种新技术的发展奠定了基础,被认为是消化内镜发展史上的又一里程碑。
2 超声内镜成为内镜医师的“第三只眼”
为克服超声波本身对骨性及气体界面不易通过的特性,弥补体表探测时出现盲区及内镜检查的局限性,内镜、超声探测仪联合装置——超声内镜(EUS)登上历史舞台。
1980年,美国马格诺(Magno)和格林(Green)最先使用内镜与超声结合的电子线型超声胃镜进行实验,并获得成功。随着超声探头的微型化,超声内镜的临床应用变成现实。30年的迅速发展已使之成为一种成熟的内镜诊断技术,使内镜医师的视野超越肉眼限制、拓展到表层组织以下。
目前,超声胃镜、超声肠镜及腹腔镜下超声系统已成功用于临床,尤其是超声内镜引导的细针抽吸术(FNA)等技术可以获取细胞学或组织学标本,对肿瘤TNM分期、黏膜下肿瘤以及胆胰疾病的鉴别诊断有重要意义,极大提高了消化系肿瘤诊断率。
近年,EUS在内镜治疗中的作用日益提高,EUS引导的引流术、腹腔神经节阻滞、放射性125I粒子置入术和顺行胆胰管手术等技术蓬勃发展。
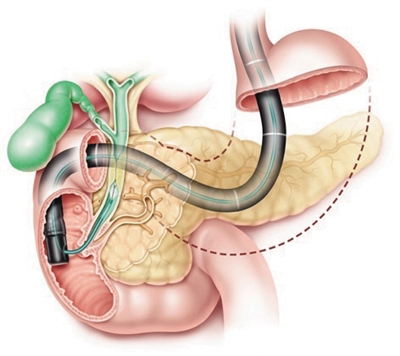
3 ERCP将诊断和治疗融为一体
1968年梅克恩(Mecune)等首次在《外科学年鉴》(Ann Surg)报道了内镜下逆行胰胆管造影术(ERCP),1973年卡瓦(Kawai)等率先报道采用推式刀进行括约肌切开,1974年克拉森(Classen)和德姆林(Demling)应用拉式弓形刀成功进行乳头切开,这标志着治疗性ERCP技术的诞生。
经过不断发展,ERCP已成为融诊断和治疗于一体的完整的学科体系。近30年来,ERCP相关新器械和新技术不断出现。经内镜下十二指肠乳头括约肌切开术(EST)目前已成为胆总管结石的主要治疗手段;经内镜下十二指肠鼻胆引流(ENBD)已成为胆道梗阻减黄的主要技术;内镜下胆管塑料支架引流术(ERBD)已广泛应用于良、恶性胆管狭窄的内镜治疗。
4 胶囊内镜和小肠镜涉足内镜检查“禁区”
曾几何时,小肠还是内镜检查无法涉足的“禁区”,很多小肠疾病只能依靠剖腹探查或术中内镜等创伤巨大的方法得以诊治。1981年,以色列国防部工程师艾登(Iddan)基于导弹遥控摄像装置的专业背景,萌生研制无线内镜的设想。在1994年的世界胃肠病大会上,Iddan结识了怀有相似创意的英国医生斯温(Swain)。两人迅速成立技术团队,1999年推出胶囊内镜原型,2001年投入临床使用。
这一产品在全世界引起了巨大反响,成为小肠疾病的一线诊断工具。此后,食管胶囊内镜、结肠胶囊内镜也相继问世。胶囊内镜技术开启了消化内镜的无线时代,孕育着极大的发展潜力。目前,通过磁控原理实现内镜医师主动控制胶囊内镜进行胃部检查的技术已完成前期研发,进入临床试验阶段。
除胶囊内镜外,小肠镜也是小肠疾病诊疗的新发明。2002年,日本学者山本博德与富士写真光机株式会社共同研制出双气囊电子小肠镜。双气囊电子小肠镜在内镜构造和进镜方式上都进行了改良,其不仅能够观察全部小肠,还能在检查过程中进行活检、止血、息肉切除、注射等治疗。
此后,单气囊小肠镜、螺旋式小肠镜也相继问世。小肠镜与胶囊内镜的应用,将小肠疾病的诊治提升到一个新高度。
5 放大内镜和显微内镜
实现对黏膜微观结构的观察
放大内镜 诊断内镜是治疗内镜的基础,高清晰度电子内镜的出现使我们肉眼对微小病变的观察得到了巨大的改进,明显地提高诊断准确率。放大内镜可通过变焦的方法,实现对黏膜表面微观结构的观察和研究。
自1975年日本多田等提出并研制放大内镜以来,经过30余年的改进,现在的新型放大内镜能够放大图像60~150倍,可以观察发生于胃肠道黏膜的腺体及绒毛的各种病理学改变。
染色内镜 又被称为色素内镜,其通过染料对胃肠道黏膜染色,使病变与周围正常黏膜对比增强,提高病变检出率。放大色素内镜将放大内镜和组织化学技术结合,明显提高对微小病变、微小结构的观察和判断,从而鉴别正常上皮、增生上皮、异型上皮和上皮性肿瘤,并判断肿瘤浸润深度和范围,为正确选择内镜下黏膜切除或外科治疗提供证据。
近年出现的电子染色技术是在色素染色的基础上,应用光学成像技术显示黏膜微小结构或血管,有代表性的是窄带滤波成像技术(NBI)、智能电子分光技术(FICE)。
电子染色技术具有放大内镜和色素染色的双重作用,是单独应用物理技术观察微小结构的又一次进步,已在临床上使用。
共聚焦显微内镜 共聚焦显微内镜是在标准电子内镜的头端整合了激光共聚焦显微镜,每次扫描光学层面厚度为7 μm,深度达0~250 μm,可观察范围包括上皮细胞、细胞外基质和基底膜、结肠隐窝结构、血管和红细胞等。
因此,共聚焦显微内镜在许多方面可代替活检及体外染色的传统病理学检查,具有广阔的发展前景。
6 内镜下微创介入治疗改变当今医疗格局
30年来,以内镜诊疗技术为代表的微创介入治疗在消化系统疾病中的作用越来越大。与外科手术相比,介入治疗技术具有操作相对简便、创伤性小、可重复性强等优点,改变了当今的医疗格局。近年,内镜下黏膜切除术(EMR)、内镜下黏膜下层剥离术(ESD)、经口内镜下肌切开术(POEM)以及别开生面的经自然腔道内镜手术(NOTES,图8)等一大批新技术涌现。
EMR和ESD技术诞生于日本,已成为全球公认的消化道早期黏膜癌的常规治疗方法。EMR适用于≤20 mm的早期癌及平坦型腺瘤;直径更大者可用分片切除术;较小者亦可用透明帽辅助进行。2001年,日本学者报道了切割法内镜下黏膜切除术(Cutting EMR)用于切除巨大平坦型早期胃癌。
POEM术是在内镜直视下彻底切断食管下端环形肌层,该手术于2009年由日本学者井上首次应用于临床,既克服了传统内镜下气囊扩张、支架置入、肉毒素注射及药物治疗等疗效不佳的弱点,又避免患者行外科手术造成的巨大创伤,现已经成为治疗贲门失弛缓症的首选方法。在POEM技术的基础上,黏膜下隧道肿瘤切除术(STER)也在逐渐发展。
NOTES是指经人体空腔脏器的自然开口进入体内,穿越管壁进行手术的一种全新理念的手术。NOTES技术可追溯到早期的结肠镜下阑尾切除术(1976年)、经皮胃镜下胃造瘘术(1980年)等,是应用经自然管壁行内镜手术的初步尝试,正是这些技术的积累逐步启发了学者越过胃肠管壁进行手术操作。1994年,威尔克(Wilk)首次提出NOTES的概念,但直到2004年卡洛(Kalloo)等成功对猪进行内镜下经胃途径腹腔探查和肝活检手术才证实了其可行性。同年,饶(Rao)等首次尝试了在人体上施行经胃阑尾切除术。令人鼓舞的是在2007年,美国贝斯勒(Bessler)和法国马尔斯科(Marescaux)等先后将NOTES技术成功地应用于临床。
NOTES具有创伤小,恢复快等优点,继传统剖腹手术、腹腔镜手术之后,有望成为第三代外科手术方式,引领微创外科学发展。
过去30年,理念不断更新
回顾30年,消化内镜技术实现了历史性突破,发展成完整的体系,已达到“无孔不入、无孔造孔而入”的境界,使内镜医师能在无创或微创的条件下进行诊断与治疗。可以说,消化内镜的发明与创新已经将消化疾病的诊断与治疗带入崭新的境地。
新技术常发轫于某些先行者的创新思维,而新技术的发展和普及则往往推动既有理念和观点的更新。30年来,内镜技术的发展、临床和基础研究的深入不断促进消化内镜学的进步,也为人类的健康作出巨大贡献。
长期以来,“早发现、早治疗”一直是医生美好的愿望,但目前我国消化内镜检出的很大一部分病变都是晚期肿瘤。在欧美和日本,过去30年间随着内镜筛查、内镜监测等概念应运而生,癌前病变和早癌的检出、治疗极大提高患者的生存率和生活质量。在这一点上,欧美和日本的经验值得我们借鉴。
例如,结直肠癌一直是欧美国家高发的肿瘤,为提高其早期诊疗,各国均采取各种筛查手段。自2001年起,美国最大的医疗保险系统(Medicare)开始覆盖结肠镜筛查,自此,结肠镜成为美国广泛推行的筛查方法。近年,多项大样本、长时间随访的研究均证明了结肠镜对结直肠癌的筛查价值。
2012年《新英格兰医学杂志》发表了一项对结肠镜息肉切除术影响直肠癌死亡率的相关研究。研究纳入1980-1990年美国全国息肉研究项目(National Polyp Study,NPS)所有接受结肠镜检的息肉(腺瘤型或非腺瘤型)患者,随访23年。结果表明,与全国死亡参数相比,接受结肠镜下息肉切除术的患者标准死亡率比值为0.47(95%可信区间0.26~0.80),提示死亡率下降53%。美国癌症统计报告显示,2002-2005年,美国结肠癌发病率每年下降4%,2005-2009年每年下降2.4%。
转化医学是近年来方兴未艾的新概念,但回顾消化内镜的发展历史我们可以发现,消化内镜领域一直在实践“转化”这一理念。消化内镜与工程技术联系非常紧密,其每一项重大突破,都堪称转化医学的典范。近年来,通过医工合作,新技术不断涌现。
例如,在超声内镜(EUS)领域,组织弹性成像技术根据人体不同组织受压后的变形差别,将不同硬度以不同彩色显示出来,第二代EUS弹性成像能够对组织声学特征进行定量分析;数字图像处理技术(DIP)通过提取EUS图像纹理特征,实现计算机辅助EUS进行定量诊断;造影增强EUS通过血流信号的不同进行疾病的诊断,正常胰腺及不同胰腺疾病之间可显示不同的增强模式、时相特点及增强强度分级,为胰腺病变的鉴别诊断提供了一种新手段。[


评论